Ako zvýšiť dostupnosť zdravotnej starostlivosti?
Pridané: 21. 04. 2021
PRINT, dátum:21.4.2021, zdroj: Lekárnické listy
Zrod nového liečiva – objav molekuly, vrátane biologickej liečby, si vyžaduje obrovské úsilie nielen výskumníkov, vedcov, ale aj významné investície výrobcov. Následne, po splnení prísnych požiadaviek regulačných inštitúcií, a cez zložitú spleť logistických transakcií sa už finálny liek dostáva k cieľu svojho určenia – k pacientovi, odkázanému na liečbu svojho ochorenia.
Molekuly liečiv, t. j. účinných látok, sa získavajú z prírodných zdrojov, syntetickou cestou alebo pomocou biotechnológie. Akonáhle sa objaví potenciálne zaujímavá molekula, výrobca si ju môže patentovať. Priemerná dĺžka patentovej ochrany originálnej (referenčnej) molekuly lieku trvá 20 rokov, pričom môže byť predĺžená o ďalších 5 rokov dodatkovým ochranným osvedčením. Farmaceutické produkty môžu byť chránené aj viacerými patentami, niekedy aj 30-timi alebo 40-timi, ktoré produkt čo najviac chránia pred konkurenciou. Aj po skončení platnosti patentu na zloženie účinnej látky lieku môžu výrobcovia predlžovať exkluzivitu, napríklad získaním nových dôkazov alebo rozšírením, resp. pridaním novej indikácie.
Po vypršaní patentovej ochrany originálneho lieku prichádzajú na trh ich cenovo výhodnejšie alternatívy vo forme generických liekov. Všetky registrované lieky, či už originálne alebo generické, musia spĺňať rovnako prísne štandardy čo sa týka kvality, bezpečnosti a účinnosti.
Garantom ich kvality, bezpečnosti a účinnosti sú štátne inštitúcie, u nás je to Štátny ústav pre kontrolu liečiv (ŠÚKL) a na úrovni EÚ je to Európska lieková agentúra (EMA). Generické lieky podliehajú nielen prísnym predpisom EÚ, ale aj vnútroštátnym požiadavkám, upravujúcim ich schvaľovanie, kvalitu, výrobu (GMP) a postmarketingový dohľad (farmakovigilancia), s cieľom zabezpečiť najvyššiu úroveň bezpečnosti, kvality a účinnosti. Náš priemysel je viazaný plniť tieto požiadavky, a je tiež v pravidelnom dialógu s európskymi a národnými regulačnými orgánmi s cieľom udržiavať vysoké štandardy pre Európu a presadzovať tieto normy globálne.
Generické lieky tvoria jadro poskytovania verejnej zdravotnej starostlivosti v liečbe nielen akútnych, ale aj chronických ochorení, od kardiovaskulárnych ochorení cez cukrovku až po onkologické ochorenia. Nie je všeobecne známe, že väčšina používaných liekov na liečbu rakoviny, vrátane liekov určených pre podpornú liečbu, sú práve generické lieky. V rámci onkologickej liečby väčšina chemoterapeutík, hormonálnych terapií a cielenejších liečebných postupov (ako súčasť liečebných protokolov) je k dispozícii vo forme generických liekov. Účinná liečba rakoviny je často podmienená aj dostupnosťou podpornej starostlivosti pri liečbe rôznych symptómov ochorenia, vedľajších účinkov liečby rakoviny a optimálneho dodržiavania liečebných cyklov, ako sú lieky proti nevoľnosti, depresii, úzkosti, ako aj liečba bolesti a infekčných chorôb.

Nepretržitá dostupnosť liekov na rakovinu je spoločným záujmom a zodpovednosťou platcov (zdravotných poisťovní), regulačných orgánov a predstaviteľov dodávateľského reťazca zameraného na pacienta. Práve generické lieky v starostlivosti o liečbu pacientov s onkologickými ochoreniami by sa mali považovať za príležitosť na zvýšenie dostupnosti liečby pre pacientov a prevenciu nedostatku liekov prostredníctvom väčšieho výberu. V ére stúpajúcich požiadaviek na zdravotnícke služby a obmedzených financií zároveň na európskej úrovni, podľa údajov Medicines for Europe (1), „za posledných desať rokov generické lieky zvýšili prístup k liekom o viac ako 100 % v 7 kľúčových terapeutických oblastiach bez navýšenia celkových nákladov na liečbu. Milióny európskych pacientov profitovali z lepšieho prístupu k terapiám, ktoré predstavujú zlatý štandard v dôsledku tejto transformácie“.
Je neuveriteľné, že na európskej úrovni generické lieky čerpajú iba veľmi malú časť rozpočtu na zdravotnú starostlivosť. 67 % receptov vydávaných liekov v Európe je generických liekov, čo predstavuje iba 29 % celkových výdavkov na lieky (1).
Bez konkurencie výrobcov generických liekov by táto úroveň prístupu stála Európu každý rok ďalších 100 miliárd eur. Podiel generických liekov v liečbe najmä chronicky chorých pacientov na Slovensku predstavuje 56 % pacientodní (2), angl. day of treatment, ktoré odčerpávajú iba 19 % z celkových nákladov na lieky hradených z verejných zdrojov (3).
Významnú bariéru ich širšieho využívania predstavuje preregulovaný systém získania úhrad, najmä v zmysle trojprahových vstupných podmienok, pretrvávajúcej výnimky z fixného doplatku pre lieky, existujúceho systému referencovania liekov, ktoré žiaľ prispievajú k prehĺbeniu netransparentného a nepredvídateľného legislatívneho prostredia.
Čoraz častejšie sa stretávame s ďalším termínom vo vzťa - hu ku generickým liekom, a to s liekmi s pridanou hodnotou (Value added medicine – VAM). Napriek doteraz nevyužitému výskumnému potenciálu predstavujú radikálnu zmenu pre farmaceutický priemysel a to v reálnom časovom horizonte. Dobre známe účinné látky za využitia nových technológií skĺbia špecifickú, personalizovanú potrebu nielen pacienta, ale aj lekára. Otvárajú nový horizont najmä pre tých pacientov, ktorí postrádajú lepšiu kvalitu života pri ich ochorení a rozhodli sa prebrať zodpovednosť za svoje zdravie do vlastných rúk.
Lieky s pridanou hodnotou predstavujú nový potenciál na optimalizáciu existujúcich terapií s príležitosťou inovovať lieky obsahujúce už dobre známe liečivá, napr. v zmysle získania nových, doteraz neschválených indikácií, zmenou dávkovacej schémy, novej cesty podania liečiva, kombináciou dvoch a viac už známych liečiv (tzv. fixné kombinácie – znižujú záťaž pacienta z užívania množstva liekov, navyše minimalizujú riziko omylu a nesprávneho užívania lieku), reformuláciou – pridaním novej technológie aplikácie.
Pre pacienta takáto pridaná hodnota liečby, podporujúca adherenciu pacienta k liečbe a dodržiavanie liečebného režimu, môže významným spôsobom zlepšiť kvalitu života pacienta. Lieky s pridanou hodnotou okrem lepšieho prístupu k liečbe ponúkajú aj flexibilitu pri výbere terapie. V neposlednom rade významnou mierou prispievajú k udržaniu rovnováhy medzi reálne dostupnou inováciou a vysoko kvalitnou zdravotnou starostlivosťou.
Práve zmena modelu liečby pacienta, ktorú priniesla pandémia COVID-19, dramaticky ovplyvnila zaužívaný prístup k zdravotnej starostlivosti. Nedostatočná dostupnosť ambulantnej, ako aj k nemocničnej starostlivosti, rýchly prechod na digitálne konzultácie a vzdialené monitorovanie pacientov, kladie ešte väčší dôraz na nevyhnutnosť zlepšenia ambulantnej, mimo nemocničnej starostlivosti.
Práve lieky s pridanou hodnotou môžu znamenať prínos pre zdravotný systém v rámci nového modelu starostlivosti o pacienta, ako napr. samo-injektovateľná subkutánna formulácia, liek s predĺženým uvoľňovaním liečiva, pomôcka monitorujúca liečivo, nový inhalátor s obsahom známeho liečiva na liečbu COPD.
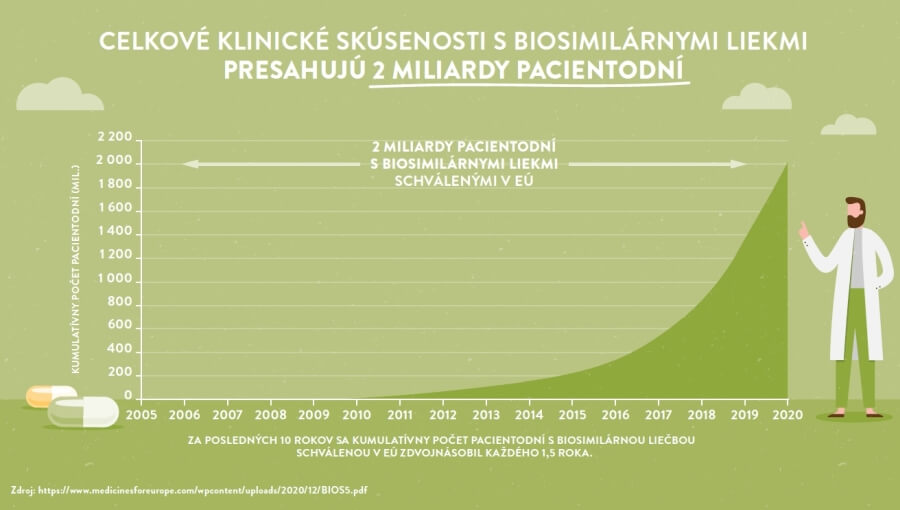
S cieľom vyriešiť naliehavú potrebu lepšieho prístupu k biologickej liečbe v Európe, sú riešením biosimilárne lieky, ktoré už od roku 2006 významne zvyšujú prístup pacientov k tejto vysoko kvalitnej liečbe. Proces hodnotenia biosimilárnych liekov v rámci EÚ prináleží Európskej liekovej agentúre (EMA). Rozhodnutie o uvedení lieku na trh v EÚ vydáva Európska komisia. Rozhodnutie komisie platí pre všetky členské štáty v EÚ dňom vydania rozhodnutia. Na biologicky podobné lieky sa vzťahujú rovnako prísne požiadavky na farmakovigilanciu, ako na všetky ostatné biologické lieky v EÚ. Od prvého schválenia biologicky podobného lieku v roku 2006 sa úspešne akumulovalo už viac ako 2 miliardy pacientodní (4) len v Európe, čo svedčí o bezpečnosti a účinnosti ako aj o silnom regulačnom rámci pre biosimilárne lieky navrhnutom európskymi regulačnými orgánmi. Mnohé analýzy dokazujú, že za rovnaké finančné prostriedky, vynaložené na biologickú liečbu, je možné odliečiť oveľa väčší počet pacientov, ako aj znížiť čakacie doby na liečbu a to najmä v onkológii, onko-hematológii, liečbe au toimunitných ochorení, ako aj liečby cukrovky.
Generické a biosimilárne lieky, t. j. lieky uvádzané na trh po vypršaní patentovej ochrany originálnych liekov, sú základným pilierom účinnej, bezpečnej a dostupnej liečby. Znamenajú efektívnu možnosť využitia nákladov, podporujú u držateľnosť systému a ponúkajú priestor na investovanie získaných úspor do zlepšenia zdravotnej starostlivosti o pacienta.
Literatúra:
1. www.medicinesforeurope.com/generic-medicines/our-5-pillars/
2. IQVIA – Rx Sell In databáza, 2019
3. INEKO: Analýza stavu a možností širšieho využívania generických a biosimilárnych liekov na Slovensku 2020, www.ineko.sk/clanky/publikacie
4. www.medicinesforeurope.com/wpcontent/uploads/2020/12/BIOS5.pdf
MUDr. Szádocka Terézia, MPH
GENAS - Asociácia pre generické a biosimilárne lieky